FDA認(rèn)證藥物主文件(DMF)|美國食品藥品管理局
美國FDA認(rèn)證 DMF(藥品主文件)是由人類藥物制造商,加工者,包裝者和儲存者自愿提交給FDA的機(jī)密文件。FDA DMF包含有關(guān)生產(chǎn)設(shè)施,過程,包裝,質(zhì)量控制和存儲產(chǎn)品的信息。
FDA DMF通常由活性藥物成分(API),藥物物質(zhì),藥物中間物質(zhì)和藥物包裝材料的制造商提交,美國FDA藥物主文件通常包含原料藥,賦形劑或包裝材料的成分/成分,化學(xué)成分,工藝技術(shù),質(zhì)量控制。
FDA DMF在成品藥申請人NDA,ANDA和IND中起著重要作用。因此,專家精心準(zhǔn)備文件對于成功提交至關(guān)重要,藥物主文件(DMF)是向FDA提交的文件,用于提供有關(guān)在人類藥物產(chǎn)品的制造,加工,包裝和存儲中使用的設(shè)施,過程或物品的機(jī)密詳細(xì)信息。
他們:
1.允許各方參考資料而不向其透露DMF內(nèi)容。
2.法規(guī)或法規(guī)沒有要求。
3.既不被批準(zhǔn)也不被拒絕。取而代之的是,F(xiàn)DA審查了與DMF相關(guān)的申請(例如NDA,ANDA,IND,BLA)的技術(shù)內(nèi)容。
美國藥品主文件類型
以下是FDA DMF文件類型:
I類
生產(chǎn)場所,設(shè)施,操作程序和人員(已移除FDA,不再適用)
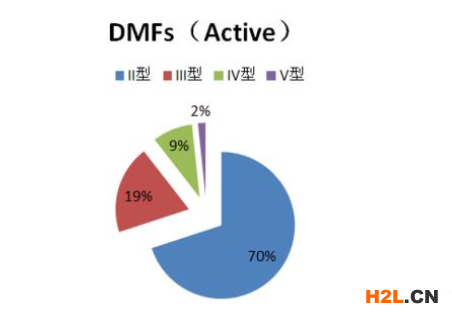
II
類用于制備上述任何物質(zhì)的藥物產(chǎn)品或物質(zhì)或中間體和/或材料。
III型
包裝材料
IV型
賦形劑或著色劑或調(diào)味劑/香精或制備中使用的材料
V型
FDA接受的參考信息
美國藥品主文件和定價:
以下是各種FDA DMF服務(wù)收取的費(fèi)用。
2-3個月內(nèi)準(zhǔn)備DMF:病房2800美元
eCTD轉(zhuǎn)換:$ 150/50頁(有折扣)
提供美國FDA認(rèn)證辦理服務(wù),主要服務(wù)產(chǎn)品有:食品、化妝品、醫(yī)療、激光的FDA注冊!
中企檢測認(rèn)證網(wǎng)提供iso體系認(rèn)證機(jī)構(gòu)查詢,檢驗檢測、認(rèn)證認(rèn)可、資質(zhì)資格、計量校準(zhǔn)、知識產(chǎn)權(quán)貫標(biāo)一站式行業(yè)企業(yè)服務(wù)平臺。中企檢測認(rèn)證網(wǎng)為檢測行業(yè)相關(guān)檢驗、檢測、認(rèn)證、計量、校準(zhǔn)機(jī)構(gòu),儀器設(shè)備、耗材、配件、試劑、標(biāo)準(zhǔn)品供應(yīng)商,法規(guī)咨詢、標(biāo)準(zhǔn)服務(wù)、實驗室軟件提供商提供包括品牌宣傳、產(chǎn)品展示、技術(shù)交流、新品推薦等全方位推廣服務(wù)。這個問題就給大家解答到這里了,如還需要了解更多專業(yè)性問題可以撥打中企檢測認(rèn)證網(wǎng)在線客服13550333441。為您提供全面檢測、認(rèn)證、商標(biāo)、專利、知識產(chǎn)權(quán)、版權(quán)法律法規(guī)知識資訊,包括商標(biāo)注冊、食品檢測、第三方檢測機(jī)構(gòu)、網(wǎng)絡(luò)信息技術(shù)檢測、環(huán)境檢測、管理體系認(rèn)證、服務(wù)體系認(rèn)證、產(chǎn)品認(rèn)證、版權(quán)登記、專利申請、知識產(chǎn)權(quán)、檢測法、認(rèn)證標(biāo)準(zhǔn)等信息,中企檢測認(rèn)證網(wǎng)為檢測認(rèn)證商標(biāo)專利從業(yè)者提供多種檢測、認(rèn)證、知識產(chǎn)權(quán)、版權(quán)、商標(biāo)、專利的轉(zhuǎn)讓代理查詢法律法規(guī),咨詢輔導(dǎo)等知識。
本文內(nèi)容整合網(wǎng)站:百度百科、搜狗百科、360百科、知乎、市場監(jiān)督總局 、國家認(rèn)證認(rèn)可監(jiān)督管理委員會、質(zhì)量認(rèn)證中心
免責(zé)聲明:本文部分內(nèi)容根據(jù)網(wǎng)絡(luò)信息整理,文章版權(quán)歸原作者所有。向原作者致敬!發(fā)布旨在積善利他,如涉及作品內(nèi)容、版權(quán)和其它問題,請跟我們聯(lián)系刪除并致歉!