01、歐洲CE認證簡介
根據MedTec Europe統計,2022年歐洲醫療器械市場規模約為1350億歐元,約占全球市場的27%,是僅次于美國的第二大醫療器械市場。
自2021年5月起,醫療器械制造商必須遵守歐盟醫療器械法規2017/745而不是醫療器械指令93/42/EEC,才能獲得CE標志批準。因此,醫療器械必須根據MDR進行分類。

?為了證明您的設備符合這些CE指令的基本要求,您需要在其上貼上CE標志。您的產品需要通過CE認證標記過程。后者的方向取決于您的醫療器械類別和您選擇的合格評定途徑。您的醫療設備的具體特性將決定其類別,以及對患者的風險程度。例如,預期用途、侵入性以及局部與全身效應等特征。
02、醫療器械CE認證所需程序及流程
(一)確認出口國家
(二)確認產品類別及歐盟相關產品指令
(三)指定“歐盟授權代表( 歐盟授權代理 ) ”(Authorized Representative)
(四)確認認證所需的模式(Module)
(五)采用 " 自我聲明 " 模式還是 " 必須通過第三方認證機構"
(六)建立技術文件 (Technical Files) 及其維護與更新
(一)確認出口國家
若出口至歐洲經濟區EEA包括歐盟EU及歐洲自由貿易協議EFTA的 30 個成員國 中的任何一國,則可能需要CE認證。
(二)確認產品類別及歐盟相關產品指令
根據歐洲框架,醫療器械分為四類:I類、IIa類、IIb類和III類。III類醫療器械的風險最高。今天,由于新監管系統的更嚴格規則,許多設備的類別發生了變化。之前他們會被歸入IIa或IIb類,但現在他們將被歸入III類。如果您的醫療設備屬于I類以外的任何其他類別,您必須向認證機構提供證明,證明您的產品符合相應CE指令的基本要求。
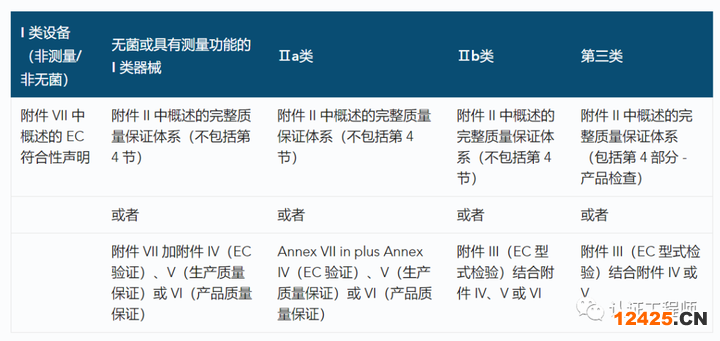
1.第一類醫療器械CE
醫療器械類I的風險最低。此類設備的制造商可以選擇三種可能的CE標記途徑中的一種。在這方面,他們應該考慮以下幾點:
(1)如果醫療器械是否是無菌的,例如個人防護套件;
(2)醫療器械是否具有測量功能,如聽診器;
(3)如果它不是無菌的,也不是測量的,例如矯正眼鏡。
注意:如果您的產品是I類產品,并且它不是無菌或測量設備,那么您只需對其進行自我認證,并通過書面聲明正式聲明其符合MDD的適用要求。如果它是無菌或測量醫療設備,那么您將需要認證機構評估。
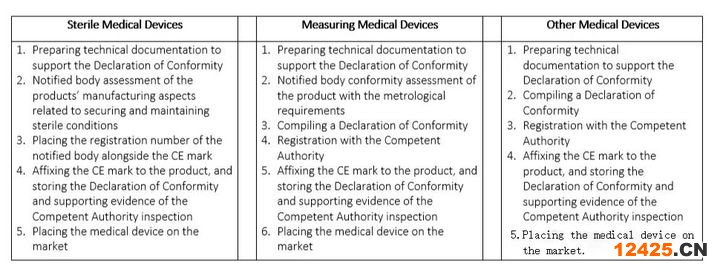
表1:I類醫療器械的CE認證標志路線
2.IIa類醫療器械CE
IIa類醫療器械可能是手術手套、助聽器、診斷超聲機等。它們通常構成中低風險。患者應短期使用,不超過30天。如果您是IIa類醫療設備的制造商,您必須支持您的聲明符合認證機構評估。只有這樣,您才能將您的產品投放市場。有四種可能的途徑可以讓您的產品獲得CE標志,根據產品的類型(即是否無菌)分為兩組。

表2.IIa類醫療器械的CE標志路線
3.IIb類醫療器械CE
IIb類器械包:括醫療設備,例如長期矯正隱形眼鏡、手術激光、除顫器等。它們是中高風險設備,患者可能會使用它們超過30天。如果您的產品屬于IIb類,類似于IIa類的程序,您將需要指定機構來評估您的技術文檔是否符合醫療器械指令。特定CE標志路線的選擇將再次取決于您的產品類型。
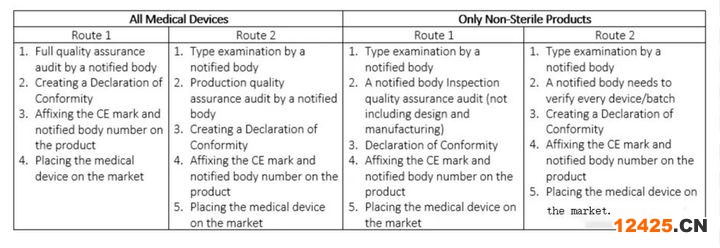
表3.IIb類醫療器械的CE標志路線
4.第三類醫療器械CE
在該類別中,所有醫療設備都具有最高的風險,并且需要在其生命周期內進行永久監控。有專門的機構負責對產品進行監測。例如,此類裝置是心血管導管、動脈瘤夾、髖關節植入物、人工心臟瓣膜等。在這里,以及在II類中,醫療器械的合格評定可能包括對技術文件的審核和質量體系/產品檢查,并側重于器械設計和生產的一個或多個方面。
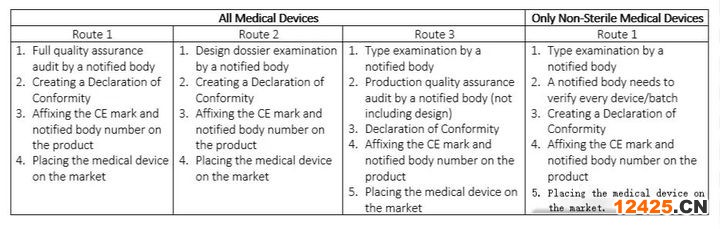
表4 類醫療器械的CE標志路線
(三)指定“歐盟授權代表( 歐盟授權代理 ) 為了能確保前述CE標志 (CE Marking )認證實施過程中的4 項要求得以滿足,歐盟法律要求位于30 個 EEA 盟國境外的制造商 必須在歐盟境內指定一家歐盟授 權代表 ( 歐盟授權代理 ) (AuthorizedRepresentative),以確保產品投放到歐洲 市場后,在流通過程及使用期間產品“安全”的一貫性;技術文件 (Technical Files)必須存放于歐盟境內供監督機構隨時檢查;對被市場監督機構發現的不 合 CE要求的產品、或者使用過程中出現事故但是已加貼CE標簽的產品,必須 采取補救措施。(比如從貨架上暫時拿掉,或從市場中永久地撤除);已加貼 CE標簽之產品型號在投放到歐洲市場后,若遇到歐盟有關的法律更改或變化,其后續生產的同型號產品也必須相應地加以更改或修正, 以便符合歐盟新的法律 要求。
(四)確認認證所需的模式(Module)
對于幾乎所有的歐盟產品指令來說,指令通常會給制造商提供出幾種 CE認證 (Conformity Assessment Procedures)的模式 (Module) ,制造商可根據本身的情況量體裁衣,選擇最適合自已的模式。一般地說,CE 認證模式可分為以下9種基本模式 :
1.Module A: internal production control
模式 A: 內部生產控制 ( 自我聲明 )
2.Module Aa: intervention of a Notified Body
模式 Aa: 內部生產控制 加第 3 方檢測
3.Module B: EC type-examination
模式 B: EC型式試驗
4.Module C: conformity to type
模式 C: 符合型式
5.Module D: production quality assurance
模式 D: 生產質量保證
6.Module E: product quality assurance
模式 E: 產品質量保證
7.Module F: product verification
模式 F: 產品驗證
8.Module G: unit verification
模式 G: 單元驗證
9.Module H: full quality assurance
模式 H: 全面質量保證
基于以上幾種基本模式的不同組合,又可能衍生出其它若干種不同的模式。一 般地說,并非任何一種模式均可適用于所有的產品。換言之, 也并非制造商可以隨意選取以上任何一種模式來對其產品進行CE認證。
(五)采用“自我聲明”模式還是“必須通過第三方認證機構”
風險水平 (Risk Level) 較低 (Minimal Risk)
歐盟的產品指令允許某些類別中風險水平 (Risk Level) 較低 (Minimal Risk) 的產品之制造商選擇以模式A:“內部生產控制 ( 自我聲明 ) ”的方式進行CE 認證。
風險水平較高的產品必須通過第三方認證機構 NB(Notified Body) 介入。
對于風險水平較高的產品,其制造商必須選擇模式 A以外的其它模式, 或者模式A外加其它模式來達到 CE 認證。也就是說,必須通過第三方認證機構NB(Notified Body)介入。
模式 A 以外的其它模式的認證過程中,通常均需要至少一家歐盟認可的認證機構 NB 參于認證過程中的一部分或全部。根據不同的模式,NB則可能分別以:來樣 檢測,抽樣檢測,工廠審查,年檢,不同的質量體系審核,等等方式介入認證過 程,并出具相應的 檢測報告,證書等。
目前,已經有 1200 多家認證機構獲得歐盟認可, 這些認證機構中的絕大多數位 于歐盟盟國境內。通常情況下, 一家 NB僅被歐盟授權可針對某一類或幾類產品 進行某一或幾種模式下的認證。換言之,一家歐盟授權的認證機構并不可能針 對所有的產品種類進行認證,即使對其被授權的產品種類,通常情況下也并非 被授權所有的模式。對于每一個歐盟的產品指令,通常都有一個針對該產品指 令的授權認證機構NB名錄。
(六)建立技術文件 (Technical Files)及其維護與更新
歐盟法律要求,加貼了 CE標簽的產品投放到歐洲市場后, 其技術文件 (TechnicalFiles) 必須存放于歐盟境內供監督機構隨時檢查。技術文件中所包涵的內容若有變化,技術文件也應及時地更新。
"技術文檔"是歐盟醫療器械指令中很重要的一個事項, 它的目的是要求企 業準備充份的技術資料和證明, 供主管機關抽查, 或發生訴訟糾紛時使用。各歐盟指令對于 " 技術檔案 " 的要求有所差別, 在這里謹以中國出口企業最 常用的“醫療器械”的要求為例,加以說明。
醫療器械指令 93/42/ EEC要求 " 技術檔案 " 可能包含下列項目:
A、企業的質量手冊和程序文件
B、企業簡介及歐洲代理名稱、聯系方式
C、CE符合性聲明(或稱自我保證聲明, 若該產品是和其它設備聯合運用, 則應有整體符合基本要求的證明材料)
1.產品名稱、分類及引用標準條款的簡要描述
2.產品概述(包括類型和預期用途)
a) 產品的歷史沿革
b) 技術性能參數
c) 產品配合使用的附件、配合件和其它設備清單
d) 產品的圖示與樣品
e) 產品所用原材料及供應商
3.使用該產品的調和標準 / 或其它標準
4.風險分析評估結論和預防措施( EN1441 產品服務危險分析報告)
5.生產質量控制
a) 產品資料和控制文檔(包括產品生產工藝流程圖)
b) 產品的滅菌方法和確認的描述
c) 滅菌驗證
d) 產品質量控制措施
e) 產品穩定性和效期的描述
6.包裝和標識
a) 包裝材料說明
b) 標簽
c) 使用說明書
中企檢測認證網提供iso體系認證機構查詢,檢驗檢測、認證認可、資質資格、計量校準、知識產權貫標一站式行業企業服務平臺。中企檢測認證網為檢測行業相關檢驗、檢測、認證、計量、校準機構,儀器設備、耗材、配件、試劑、標準品供應商,法規咨詢、標準服務、實驗室軟件提供商提供包括品牌宣傳、產品展示、技術交流、新品推薦等全方位推廣服務。這個問題就給大家解答到這里了,如還需要了解更多專業性問題可以撥打中企檢測認證網在線客服13550333441。為您提供全面檢測、認證、商標、專利、知識產權、版權法律法規知識資訊,包括商標注冊、食品檢測、第三方檢測機構、網絡信息技術檢測、環境檢測、管理體系認證、服務體系認證、產品認證、版權登記、專利申請、知識產權、檢測法、認證標準等信息,中企檢測認證網為檢測認證商標專利從業者提供多種檢測、認證、知識產權、版權、商標、專利的轉讓代理查詢法律法規,咨詢輔導等知識。
本文內容整合網站:百度百科、搜狗百科、360百科、知乎、市場監督總局 、國家認證認可監督管理委員會、質量認證中心
免責聲明:本文部分內容根據網絡信息整理,文章版權歸原作者所有。向原作者致敬!發布旨在積善利他,如涉及作品內容、版權和其它問題,請跟我們聯系刪除并致歉!







