一、核心澄清:中藥材 GAP 已無 “認證部門”,實行 “備案制 + 藥監監管”
中藥材 GAP 認證是哪個部門認證的?這一問題的關鍵誤區在于 “認證” 二字 ——2016 年國務院已取消中藥材 GAP 行政許可認證,現行體系為 “企業自主備案 + 藥監部門監督”。核心監管主體是國家藥監局與省級藥監局,輔以技術支撐機構(如審評查驗中心、藥檢所),形成 “國家定規則、省級抓落實、技術機構做支撐” 的三級管理體系,精準對接這些部門是備案成功的核心前提。
二、中藥材 GAP 備案核心部門及職責分工(2025 年新規版)
不同層級部門在備案、檢查、監管環節的職能差異顯著,以下為全鏈條職責明細:
|
部門層級 |
具體執行機構 |
核心職責 |
關鍵時限 |
2025 年新規亮點 |
|
國家層面 |
國家藥品監督管理局(中藥監管司) |
制定備案規則、檢查指南;建設追溯平臺;組織全國抽查 |
無固定時限,按年度部署抽查 |
中藥注射劑原料原則上需用備案藥材 |
|
國家層面 |
國家藥監局藥品認證管理中心 |
承擔備案材料形式審查、檢查員庫管理 |
20 個工作日內完成形式審查 |
新增碳足跡數據核查要求 |
|
省級層面 |
各省藥監局(藥品注冊與生產監管處) |
備案材料初審、現場檢查組織、日常監管 |
15-20 個工作日內完成初審 |
開展示范建設企業遴選(如江西第三批遴選) |
|
省級層面 |
省級審評查驗中心(如寧夏) |
制定檢查方案、實施現場檢查、出具報告 |
檢查結束后 5 日內提交報告 |
采收期開展不通知式檢查 |
|
技術支撐 |
省級藥檢所、第三方檢測平臺 |
基原鑒定、農殘 / 重金屬檢測、數據核驗 |
7-15 個工作日出具檢測報告 |
支持區塊鏈溯源數據核驗 |
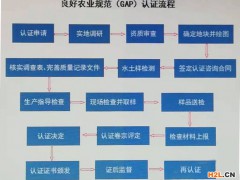
三、中藥材 GAP 備案全流程:部門對接節點拆解
備案流程的每個環節對應不同部門,精準把握對接節點可縮短備案周期 40%,具體流程如下:
3.1 五階段部門對接指南
- 準備階段(對接技術支撐機構)
-
- 向省級藥檢所申請基原鑒定(如當歸需明確基原為 Angelica sinensis),獲取《基原鑒定報告》;
-
- 委托 CMA 認證的第三方檢測平臺開展土壤、灌溉水檢測(需符合 GB 4284-2018 標準)。
- 初審階段(對接省級藥監局)
-
- 提交材料:備案申請表、基地產權證明、檢測報告等(江西要求含近 5 年抽檢合格證明);
-
- 部門對接:省級藥監局 “中藥材 GAP 工作專班” 開展初審,材料不全需 5 日內補齊。
- 檢查階段(對接審評查驗中心)
-
- 檢查組織:省級審評查驗中心組建 3-5 人檢查組(含 GAP 檢查員與專家);
-
- 現場核查:重點檢查種質資源、采收記錄、加工規程(寧夏要求覆蓋 300 余項指標)。
- 公示階段(對接省級藥監局)
-
- 綜合評定:審評查驗中心出具報告后,省級藥監局審核并公示(公示期不少于 5 個工作日);
-
- 異議處理:公示期內接受投訴舉報,由省級藥監局組織復核。
- 監管階段(對接國家 + 省級藥監部門)
-
- 日常監管:省級藥監局每兩年開展 1 次延伸檢查;
-
- 全國抽查:國家藥監局每年按 10% 比例抽查備案基地。
3.2 關鍵材料提交部門與要求
|
材料名稱 |
提交部門 |
核心要求 |
常見駁回原因 |
|
基原鑒定報告 |
省級藥監局 |
需省級藥檢所蓋章,明確基原準確性 |
基原描述模糊(如 “人參” 未細分品種) |
|
產地加工規程 |
省級審評查驗中心 |
附傳統經驗或研究數據支持 |
無趁鮮切制溫度 / 時間參數記錄 |
|
追溯體系證明 |
國家藥監局認證管理中心 |
需接入國家中藥追溯平臺 |
溯源數據未覆蓋采收 - 加工全環節 |
四、常見問題與部門對接解決方案
4.1 高頻問題及責任部門
- Q1:備案材料被省級藥監局駁回,找誰申訴?
A:向省級藥監局 “中藥監督管理處” 提交申訴材料,附情況說明與補充證據,10 個工作日內反饋復核結果。
- Q2:現場檢查發現缺陷項,如何整改對接?
A:向省級審評查驗中心提交《整改報告》,明確整改措施與時限(輕微缺陷 30 日內完成),整改完成后由檢查組長復核。
- Q3:追溯數據無法接入國家平臺,聯系哪個部門?
A:撥打國家藥監局 “中藥追溯平臺技術支持熱線”(400-810-8881),或通過省級藥監局信息化處協調對接。
4.2 部門對接避坑指南
- ? 誤區 1:直接向國家藥監局提交備案材料?
? 糾正:需先經省級藥監局初審,跳過省級直接申報將被駁回(國家藥監局僅受理省級初審通過的材料)。
- ? 誤區 2:檢測報告隨便找機構出具?
? 糾正:必須由省級藥檢所或國家藥監局認可的第三方平臺出具,普通農業檢測報告無效。
- ? 誤區 3:日常監管僅需對接省級藥監局?
? 糾正:示范建設企業需同時對接省農業農村廳(獲取種植技術指導)、省中醫藥局(政策補貼申報)。
五、總結:找對部門是中藥材 GAP 備案的 “第一關”
中藥材 GAP 認證是哪個部門認證的?答案是 “無認證部門,全鏈條由藥監系統監管”—— 國家藥監局定規則,省級藥監局抓初審與監管,審評查驗中心做檢查,藥檢所提供技術支撐。2025 年新規下,還需對接示范建設遴選部門(如江西)與追溯平臺技術支撐部門。提前明確各環節對接機構,準備好基原鑒定、檢測報告等關鍵材料,才能高效通過備案,成為藥企優先采購的 “放心藥材” 供應方。
中企檢測認證網提供iso體系認證機構查詢,檢驗檢測、認證認可、資質資格、計量校準、知識產權貫標一站式行業企業服務平臺。中企檢測認證網為檢測行業相關檢驗、檢測、認證、計量、校準機構,儀器設備、耗材、配件、試劑、標準品供應商,法規咨詢、標準服務、實驗室軟件提供商提供包括品牌宣傳、產品展示、技術交流、新品推薦等全方位推廣服務。這個問題就給大家解答到這里了,如還需要了解更多專業性問題可以撥打中企檢測認證網在線客服13550333441。為您提供全面檢測、認證、商標、專利、知識產權、版權法律法規知識資訊,包括商標注冊、食品檢測、第三方檢測機構、網絡信息技術檢測、環境檢測、管理體系認證、服務體系認證、產品認證、版權登記、專利申請、知識產權、檢測法、認證標準等信息,中企檢測認證網為檢測認證商標專利從業者提供多種檢測、認證、知識產權、版權、商標、專利的轉讓代理查詢法律法規,咨詢輔導等知識。
本文內容整合網站:百度百科、搜狗百科、360百科、知乎、市場監督總局 、國家認證認可監督管理委員會、質量認證中心
免責聲明:本文部分內容根據網絡信息整理,文章版權歸原作者所有。向原作者致敬!發布旨在積善利他,如涉及作品內容、版權和其它問題,請跟我們聯系刪除并致歉!